Na história do estudo do cérebro, não há estrutura mais estudada do que o córtex cerebral. Uma das razões é que o nosso córtex cerebral é particularmente grande quando comparado ao de outros grandes primatas. É no córtex que acontece boa parte do processamento necessário para a nossa cognição. Assim, entender de onde vem esse córtex diferente que nós temos pode ajudar a explicar as origens desse macaco pensador. Mas até muito recentemente, nós não tínhamos muitas pistas sobre os mecanismos que levaram ao desenvolvimento deste córtex maior. Tudo mudou quando descobrimos, há menos de dez anos, algumas duplicações de pedacinhos de nossos cromossomos. Mas para entender a importância destes pedacinhos, precisamos primeiro olhar como se forma o córtex cerebral.
O córtex cerebral, como qualquer outra estrutura do sistema nervoso central, se forma a partir do tubo neural. O tubo neural é um folheto de células em divisão. Em um primeiro momento, estas células se dividindo não se diferenciam, são células tronco neurais, com capacidade de originar neurônios e células da glia. Depois de um tempo, algumas células deixam o ciclo celular, começam a se diferenciar e migram das porções mais internas do tubo em direção ao seu exterior
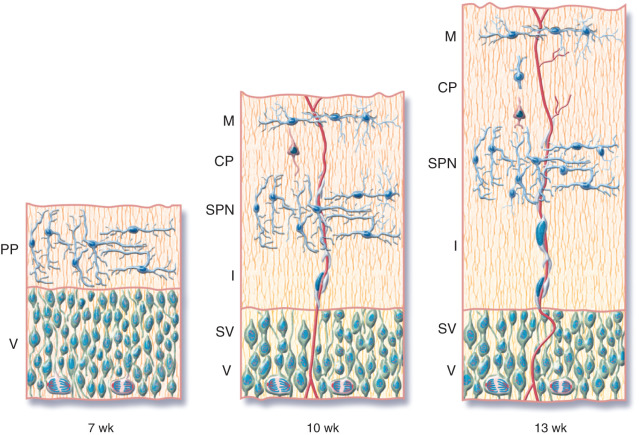
Durante o desenvolvimento, as paredes do tubo neural vão ganhando espessura, acrescentando mais e mais camadas. Após a sua migração, parte das células se diferencia em neurônios e outra parte em células da glia. Os neurônios então começam a emitir prolongamentos que podem se conectar com alvos próximos ou muito distantes. É por conta destas conexões à distância que se forma o que chamamos de substância branca, grandes regiões do nosso cérebro dedicadas à passagem de cabos conectores, os axônios. Todos estes fenômenos podem levar a um córtex maior. Se cada célula tronco neural se dividir mais vezes, gerando mais neurônios e/ou glia, estas células a mais ocuparão mais espaço. Se os neurônios formarem mais conexões, elas ocuparão mais volume e a substância branca irá também aumentar. Muitas espécies de mamíferos possuem um córtex tão grande e extenso que ele se acomoda à caixa craniana por meio de dobras em estruturas que chamamos de sulcos e giros. Qualquer modificação na expressão de moléculas que regulem estes fenômenos tem o potencial de gerar uma catástrofe, como malformações cerebrais, mas também modificações que são novidades sobre as quais a seleção natural pode operar, levando a alterações, por exemplo, na capacidade cognitiva da espécie.
As técnicas de sequenciamento de DNA sofreram uma grande revolução no começo deste século com a chegada das técnicas de sequenciamento de nova geração, do inglês next generation sequencing. Nesta tecnologia, o genoma é quebrado em pequenas sequências de DNA que são sequenciadas várias vezes. Nestas várias vezes, a mesma sequência aparece às vezes associada com nucleotídeos mais abaixo na cadeia e às vezes com nucleotídeos mais acima. Combinando a informação sobre estas relações de vizinhança, podemos montar um quebra cabeça para obter a sequência toda. Obviamente ninguém monta um genoma com bilhões de nucleotídeos no olho. Para isso, um grande esforço de desenvolvimento de ferramentas de bioinformática foi criado. Mas mesmo com todas estas ferramentas, o montar do quebra cabeça pode ser especialmente desafiador quando estas sequências são muito repetitivas ou duplicadas. Uma das soluções foi voltar a técnicas antigas para realizar o sequenciamento de cadeias de nucleotídeos longas. A outra foi investir em algoritmos melhores, à medida que fomos aprendendo sobre estas falhas. Assim, apesar de termos o primeiro genoma humano desde 2003, foi somente em 2014 que conseguimos detectar duplicações de um grupo importante de genes para os nossos cérebros. E esses genes duplicados deram o que falar.
Hoje em dia, além de termos muitos genomas de seres humanos sequenciados, temos também genomas de grandes macacos, como chimpanzés e gorilas, e grandes pedaços de genomas de hominíneos extintos, como Neandertais. A partir da comparação entre estes genomas, podemos detectar quais genes foram duplicados em nossa linhagem. Dentre os genes encontrados, alguns são expressos durante o desenvolvimento do córtex cerebral e são, assim, possíveis fontes de novidades evolutivas nessa estrutura. Isso porque hoje sabemos que o gene duplicado não sofre as mesmas pressões seletivas para manter as funções desempenhadas pelo gene ancestral. Nele pode haver modificações que eventualmente criem uma nova função. Mas o simples fato de o gene novo ser expresso em um córtex diferente não quer dizer que um causou o outro. E é aí que entram os experimentos que testam a função do gene.
Mas aqui esbarramos em um problema. Como testar o efeito de um gene novo para hominíneos se é eticamente inaceitável realizar um teste da sua função em um embrião humano? Para isso, criamos modelos que se aproximam o máximo possível do que sabemos sobre o desenvolvimento do córtex cerebral em humanos. Tomemos então aqui como exemplo o estudo de um dos genes identificados como potencial novidade na evolução do córtex cerebral, que foi chamado de ARHGAP11B. Este gene não está presente em nenhum dos grandes primatas, mas está presente em Neandertais, hominíneos de Denisova e todos os humanos modernos. O ARHGAP11B é o produto da duplicação parcial do gene ARHGAP11A. A enzima ARHGAP11A, resultante da transcrição e tradução do gene de mesmo nome, é uma enzima envolvida na sinalização intracelular. Mas ARHGAP11B perdeu esta função, pois graças à substituição de uma única citosina por uma guanina, criou-se um novo sítio para splicing que acaba por remover 55 nucleotídeos originais de seu RNA mensageiro. Esta mudança acabou por gerar uma parte completamente nova desta proteína, que perdeu sua atividade enzimática original, mas ganhou uma nova função.
Para descobrir que função é esta, Marta Florio e seus colaboradores se perguntaram se este gene específico de humanos, quando expresso em células tronco neurais do córtex cerebral em formação de camundongos, teria algum efeito. Os pesquisadores promoveram, então, a expressão artificial de ARHGAP11B no cérebro de embriões de camundongo. O que eles observaram foi que, na presença de ARHGAP11B, as células tronco neurais se dividem mais e o córtex cerebral ganha sulcos e giros, que não existem no cérebro liso desses animais. Assim, o uso de embriões de camundongo como modelo sugere indiretamente que a função nova de ARHGAP11B pode ter contribuído para a expansão do córtex de hominíneos.
Mas será que o efeito observado é uma propriedade única da expressão artificial em células de camundongo? O que aconteceria se ele fosse expresso nas células de um primata? Aí entra uma nova corrida tecnológica. A criação de um modelo animal, que atenda requisitos de um animal de laboratório, mas que seja um primata. Para isso, a espécie escolhida foi Callithrix jacchus (o sagui, ou sorin, para nós aqui no RN). Para conseguir saguis expressando ARHGAP11B, este mesmo grupo injetou um lentivírus contendo o gene e sua região regulatória em óvulos fertilizados. Assim, eles obtiveram embriões em que o gene foi incorporado ao genoma. Após isso, os embriões foram transferidos para fêmeas para a gestação. Os embriões que receberam o gene com sucesso apresentaram ampliação no número de células tronco neurais, de novos neurônios e formaram sulcos e giros no córtex cerebral, que em saguis também é liso. Assim, as evidências indiretas da participação de ARHGAP11B na expansão cortical se acumulam. A proteína possui efeitos semelhantes em progenitores corticais de espécies diferentes, não parecendo ser esta observação apenas um efeito colateral do modelo. ARHGAP11B se soma a outros genes novos de hominíneos que atuam no desenvolvimento cortical, como NOTCH2NL, cuja duplicação também causou o aumento no número de divisões que as células tronco neurais fazem, e SRGAP2C, que se tornou um inibidor da proteína produzida pelo gene original (que é um inibidor de sinapses e ramificações de neurônios). Como SRGAP2C é um inibidor de uma proteína inibidora da formação de sinapses, ela acaba sendo um estimulador de sinapses. Todos estes genes estavam presentes em Neandertais e hominíneos de Denisova. Por isso, é difícil acomodar na hipótese molecular atual a ideia preconceituosa de que nós seríamos intelectualmente superiores ou mesmo teríamos um córtex mais avantajado do que os hominíneos com os quais convivemos no último milhão de anos.
Eduardo Sequerra (UFRN)
PARA SABER MAIS:
Marta Florio, Victor Borrell e Wieland Huttner (2017) Human-specific genomic signatures of neocortical expansion. Current Opinion in Neurobiology

